Densidade na Tabela Periódica
O estudo da densidade na Tabela Periódica baseia-se apenas na análise da posição ocupada por um determinado elemento químico em um período e família.
Por Diogo Lopes Dias

PUBLICIDADE
A densidade é a relação estabelecida entre a massa da matéria e o volume que ela ocupa, sendo representada pela seguinte fórmula:
d = m
V
Quando falamos sobre os elementos químicos, também podemos abordar a densidade, já que os elementos são matérias, e a densidade é uma propriedade física da matéria. Assim, conhecendo a massa de uma amostra de um elemento e o volume ocupado por ela, conseguimos determinar facilmente sua densidade.
Quando estamos lidando com elementos químicos, temos o hábito de nos reportarmos à Tabela Periódica para verificar algumas informações e características deles. Com a densidade não é diferente! Assim, ao estudar sobre um elemento químico, podemos também analisar sua densidade a partir da Tabela Periódica.
OBS.: É importante ressaltar que a densidade é uma propriedade absolutamente experimental, ou seja, para determiná-la, é necessário pesar uma amostra e determinar o seu volume.
Como é possível estudar a densidade na Tabela Periódica?
Na realidade, ao estudar a densidade como uma propriedade periódica, é possível fazer apenas uma comparação (tendência) entre as densidades de dois ou mais elementos químicos, pois é impossível determinar a densidade de um elemento apenas analisando a Tabela Periódica. Essa comparação obviamente se baseia em dados que foram coletados em laboratório.
Para facilitar a comparação entre as densidades de elementos químicos, utilizamos uma regra que se baseia nos períodos e famílias da Tabela. A regra é a seguinte:
-
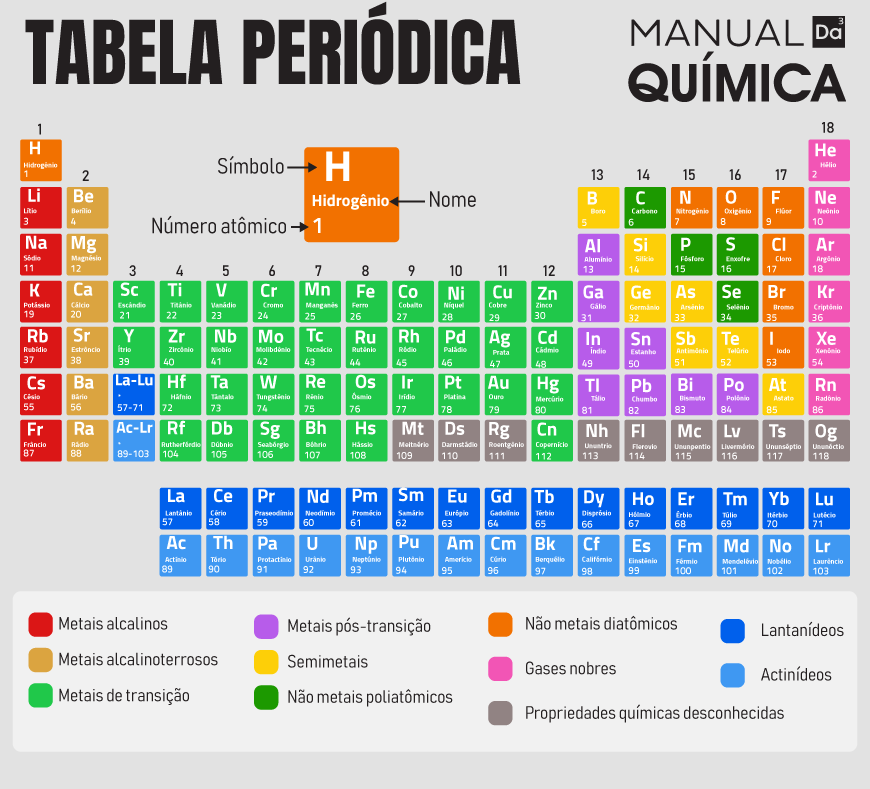
Nos períodos: a densidade dos elementos tende a crescer sempre das extremidades para o centro, ou seja, quanto mais localizado na região central da Tabela, mais denso tende a ser o elemento avaliado. Veja um exemplo:
Não pare agora... Tem mais depois da publicidade ;)
Comparando os elementos Potássio (K) e Ferro (Fe), pertencentes ao quarto período da Tabela Periódica, concluímos que o Ferro é mais denso que o Potássio por estar localizado mais ao centro.

OBS.: É impossível determinar por meio dessa regra quem seria mais denso, se o Potássio (K) ou o Criptônio (Kr), por exemplo, provando mais uma vez que a densidade é uma propriedade experimental.
-
Nas famílias: a densidade segue o aumento do número de níveis dos átomos. Assim, quanto maior o número de níveis (elemento posicionado mais abaixo do outro elemento na família), maior a densidade. Veja um exemplo:
Os elementos Boro (B) e Índio (In), pertencentes à família IIIA da Tabela Periódica, estão posicionados, respectivamente, no segundo e quinto períodos da Tabela. Sendo assim, os átomos de Boro apresentam menos níveis que os átomo de Índio. Por isso, o Índio apresenta densidade maior que a do Boro.
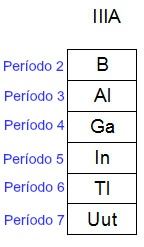
Assim, de forma geral, quando estudamos a densidade na Tabela Periódica, podemos dizer que a tendência é que ela aumente sempre das extremidades para o centro (nos períodos, seta amarela) e de cima para baixo (nas famílias, seta rosa), o que resulta no seguinte esquema geral:

Densidade aumenta sempre para o centro e para baixo na tabela periódica
OBS.: O elemento que apresenta a maior densidade em relação a todos os outros elementos é o Ósmio (Os). Esse dado é absolutamente experimental, mas temos que conhecê-lo e sempre levá-lo em consideração.
Por Me. Diogo Lopes Dias