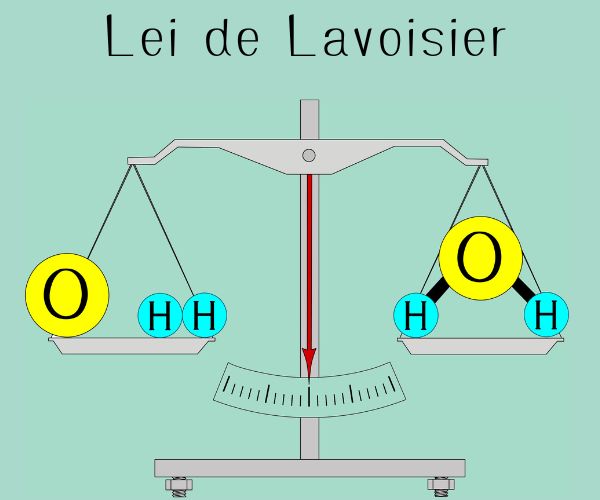
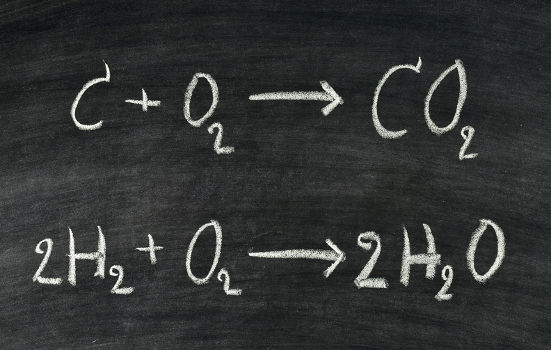Lei de Lavoisier
A lei de Lavoisier é a Lei de conservação da massa, ou seja, a massa total dos produtos é sempre igual à massa total dos reagentes.
Por Jhonilson Pereira Gonçalves
PUBLICIDADE
A lei de Lavoisier é um princípio fundamental da Química que estabelece a base para a compreensão moderna das reações químicas e da conservação da massa. Ela foi formulada por Antoine Lavoisier no final do século XVIII. Sua enunciação — “Na natureza, nada se cria, nada se perde, tudo se transforma” — reflete a ideia central de que a massa total dos reagentes em uma reação química é igual à massa total dos produtos formados. Nesse sentido, essa lei foi corroborada por meio de experimentos pioneiros, especialmente o de combustão do enxofre em um sistema fechado, proporcionando evidências cruciais para a aceitação da teoria atômica.
Leia também: Lei de Hess — a lei que enuncia sobre a variação de entalpia envolvida em uma reação química
Resumo sobre a lei de Lavoisier
- A lei de Lavoisier é um princípio fundamental da química que estabelece a base para a compreensão moderna das reações químicas e da conservação da massa.
- É também conhecida como lei da conservação das massas.
- Foi formulada por Antoine Lavoisier.
- Ficou consolidada na frase: “Na natureza nada se cria, nada se perde, tudo se transforma”.
- Tem como premissa que a massa total dos reagentes em uma reação química é igual à massa total dos produtos formados.
- Fundamenta o balanço de equações químicas.
- Mostrou-se extremamente importante para cálculos estequiométricos.
- Proporcionou uma evidência crucial para a aceitação da teoria atômica.
- Experimentos, como a combustão do enxofre, foram realizados para validá-la.
- Teve contribuição significativa para o desenvolvimento da Química moderna.
- Enquanto a lei de Lavoisier tem como foco principal a conservação da massa durante as reações químicas, a lei de Proust tem como foco principal a composição fixa dos elementos em um composto.
- Antoine Lavoisier (1743-1794) foi um químico francês. Ele é considerado o pai da Química moderna.
Videoaula sobre a lei de Lavoisier
O que diz a lei de Lavoisier?
Também conhecida como lei da conservação das massas, a lei de Lavoisier é uma importante lei da química formulada por Antoine Lavoisier, um químico francês, no final do século XVIII. Essa lei estabelece o princípio fundamental da conservação da massa em reações químicas, ou seja, a massa total dos reagentes em uma reação química é igual à massa total dos produtos formados.
A formulação clássica da lei de Lavoisier é:
“Na natureza, nada se cria, nada se perde, tudo se transforma.”
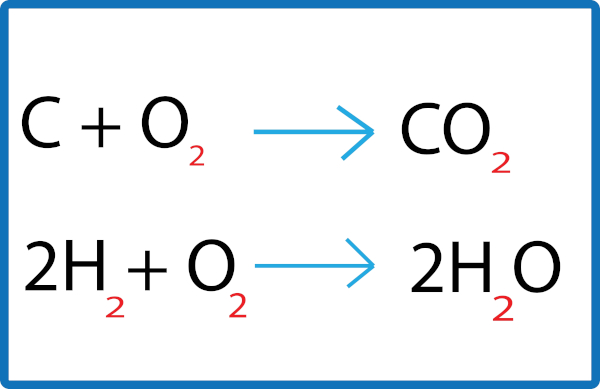
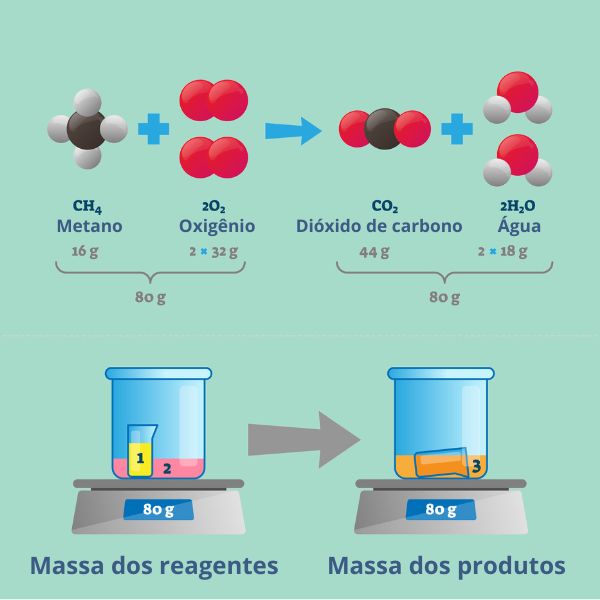
Essa afirmação significa que a quantidade total de matéria (ou massa) permanece constante antes e depois de uma reação química. Quando uma reação química ocorre, os átomos dos reagentes são rearranjados para formar novas substâncias (produtos). Apesar dessa reorganização, a massa total dos reagentes é igual à massa total dos produtos. Exemplo:
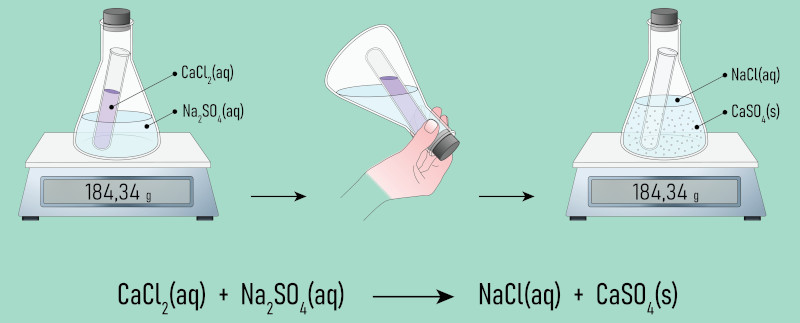
Aplicação da lei de Lavoisier
A principal aplicação da lei de Lavoisier é no balanço de equações químicas. Nesse sentido, ao escrever uma equação química, é necessário garantir que a quantidade total de átomos de cada elemento seja a mesma nos reagentes e nos produtos, pois isso é fundamental para respeitar o princípio da conservação da massa. Exemplo:
2H2 + O2 → 2H2O
Note que nos reagentes temos: 2 H2 = 4 átomos de oxigênio; 1 O2 = 2 átomos de oxigênio. Já nos produtos: 2 H2O = 4 átomos de hidrogênio; 2 átomos de oxigênio.
Nesse caso, a equação está balanceada, garantindo que a quantidade total de átomos de hidrogênio e oxigênio seja a mesma nos reagentes e nos produtos.
Outra aplicação da lei de Lavoisier é em cálculos estequiométricos para determinar quantidades relativas de reagentes e de produtos em uma reação química. Sendo assim, com base em informações sobre a massa de um reagente, pode-se calcular a massa esperada dos produtos, e vice-versa, considerando-se a conservação da massa. Exemplo: se 4 g de hidrogênio reagem com oxigênio para formar água, quanto de água é produzido?
2H2 + O2 → 2H2O
A equação mostra que 2 mol de hidrogênio produzem 2 mol de água, portanto, 4 g de hidrogênio produzirão 4 g de água.
Importante: A lei de Lavoisier é aplicada em experimentos nos quais os reagentes e produtos estão contidos em um sistema fechado, pois assim não haverá perda de reagente nem de produto para o meio externo.
Outra aplicação prática é em química analítica, em que a lei de Lavoisier é frequentemente usada para validar métodos experimentais, de modo que a comparação da massa dos reagentes conhecidos com a massa dos produtos obtidos experimentalmente ajuda a garantir a precisão e confiabilidade dos métodos analíticos.
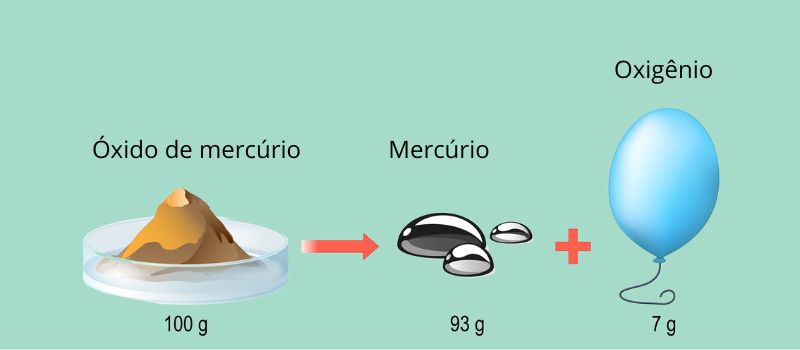
Em resumo, a lei de Lavoisier é aplicada em uma variedade de situações na Química, desde a escrita e o balanceamento de equações até os experimentos práticos que envolvem a análise de reações em sistemas fechados. Ela continua a ser uma pedra angular no entendimento das transformações químicas e é fundamental para o progresso na área da Química.
Experimento da lei de Lavoisier

Embora Antoine Lavoisier tenha realizado vários experimentos para validar a lei da conservação das massas (ou lei de Lavoisier), um dos experimentos mais notáveis foi aquele relacionado à combustão do enxofre. O experimento com combustão do enxofre ajudou a confirmar a ideia de que a massa total permanece constante durante uma reação química.
Para tal, Lavoisier realizou o experimento em um ambiente fechado para garantir que nenhum material pudesse escapar ou entrar durante a reação.
- Ele colocou uma amostra de enxofre sólido em um recipiente fechado.
- Antes de iniciar a reação, mediu a massa do enxofre e qualquer outro componente do sistema (a balança utilizada era extremamente precisa).
- O enxofre sólido foi então inflamado, iniciando a reação de combustão. Durante a combustão, o enxofre reagiu com o oxigênio presente no recipiente fechado para formar dióxido de enxofre, conforme a reação a seguir:
2S + O2 → SO2
- Após a combustão ter ocorrido completamente, Lavoisier mediu a massa final do sistema, incluindo qualquer gás formado durante a reação (a balança novamente foi utilizada para garantir medidas precisas).
Diante disso, Lavoisier observou que a massa final do sistema (que incluía o enxofre queimado e os produtos gasosos) era igual à massa inicial do sistema (que incluía apenas o enxofre sólido e o oxigênio). Além disso, ele coletou o dióxido de enxofre formado durante a reação, mostrando que o gás também contribuiu para a massa final do sistema.
Finalmente os resultados do experimento confirmaram a lei de Lavoisier, que afirma que a massa total dos reagentes em uma reação química é igual à massa total dos produtos formados. Isso implicou que nenhum átomo de enxofre foi criado ou destruído durante a combustão; apenas os átomos foram rearranjados para formar novas substâncias.
Esse experimento pavimentou o caminho para uma compreensão mais profunda da natureza das reações químicas e a conservação da matéria.
Lei de Lavoisier x lei de Proust
A lei de Lavoisier e a lei de Proust são dois importantes princípios fundamentais da Química ligados às reações químicas. Enquanto a lei de Lavoisier, ou lei da conservação das massas, foi formulada pelo químico francês Antoine Lavoisier, a lei de Proust, ou lei das proporções constantes (ou proporções definidas), foi formulada pelo químico francês Joseph Louis Proust. As duas leis foram formuladas no final do século XVIII.
A lei de Lavoisier é fundamental para a compreensão da conservação das massas durante uma reação química e estabelece que “na natureza, nada se cria, nada se perde, tudo se transforma”. Por sua vez, a lei de Proust é fundamental para o entendimento das composições químicas dos compostos e estabelece que “um composto puro sempre contém os mesmos elementos combinados na mesma proporção em massa”.
Como vimos exemplos da lei de Lavoisier ao longo de todo o texto, vamos ver, a seguir, um exemplo sobre a lei de Proust.
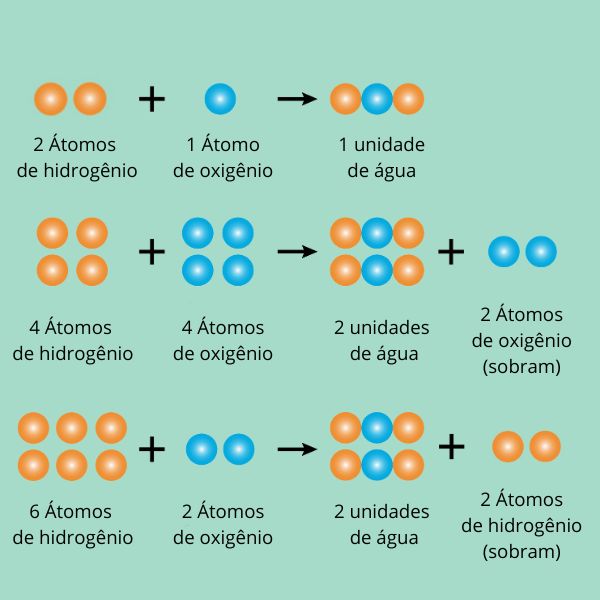
Uma molécula de água sempre será composta por 2 átomos de hidrogênio e 1 de oxigênio (H2O), ou seja, sempre será na proporção de 2:1 (hidrogênio/oxigênio). Isso vale para todas as substâncias, pois, em cada uma delas, haverá uma proporção exata que as caracteriza e as torna únicas. Vejamos isso melhor na imagem abaixo:
Diante disso, para uma melhor compreensão, vamos comparar as duas leis no quadro abaixo:
|
Aspecto |
Lei de Lavoisier (conservação das massas) |
Lei de Proust (proporções constantes) |
|
Enunciado |
“Na natureza, nada se cria, nada se perde, tudo se transforma.” |
“Um composto puro sempre contém os mesmos elementos combinados na mesma proporção em massa.” |
|
Foco principal |
Conservação da massa durante as reações químicas. |
Composição fixa dos elementos em um composto. |
|
Experimento-chave |
Combustão do enxofre em um sistema fechado. |
Estudo da composição do óxido de cobre. |
|
Evidência experimental |
A massa total dos reagentes é igual à massa total dos produtos. |
A proporção entre as massas dos elementos em um composto é constante. |
|
Contribuição para a teoria atômica |
Forneceu evidência para a ideia de que os átomos não são criados nem destruídos, apenas rearranjados. |
Reforçou a ideia de que os átomos se combinam em proporções definidas para formar compostos. |
|
Principais aplicações |
Balanço de equações químicas, cálculos estequiométricos. |
Desenvolvimento da estequiometria, entendimento das proporções em compostos. |
|
Data da formulação |
Final do século XVIII (1780) |
Final do século XVIII (1790) |
|
Relevância atual |
Fundamental na Química moderna, continua sendo princípio-chave. |
Base para a estequiometria, influência na pesquisa e compreensão de compostos. |
Em síntese, enquanto a lei de Lavoisier destaca a conservação da massa durante as reações químicas, a lei de Proust enfatiza a proporção constante dos elementos em um composto, ambas desempenhando papéis cruciais na evolução da Química.
Para saber mais detalhes sobre a lei de Proust, clique aqui.
Quem foi Lavoisier?

Antoine-Laurent de Lavoisier foi um químico francês considerado um dos fundadores da Química moderna. Ele nasceu em 26 de agosto de 1743, em Paris, França, e foi executado na guilhotina em 8 de maio de 1794, durante a Revolução Francesa. Nesse contexto, vale ressaltar que ele contribuiu significativamente para a transformação da Química de uma disciplina predominantemente empírica para uma ciência baseada em princípios fundamentais. A seguir, um pouco sobre sua vida e suas contribuições:
- Lavoisier nasceu em uma família abastada e recebeu uma educação refinada.
- Estudou Direito na Universidade de Paris, mas seu interesse pela ciência, especialmente pela Química, logo se destacou.
- Inicialmente, dedicou-se à pesquisa em várias áreas, incluindo botânica, meteorologia e Química.
- Foi eleito membro da Academia Real de Ciências em 1768.
- Foi fundamental na identificação e nomenclatura de diversos elementos químicos, incluindo o hidrogênio, o oxigênio, o azoto (nitrogênio), o enxofre e o fósforo.
- Propôs uma nova nomenclatura química mais sistemática e lógica.
- Investigou as propriedades dos gases e fez contribuições importantes para a compreensão da combustão.
- Descreveu a natureza do oxigênio e a relação entre oxigênio e combustão.
- Embora Lavoisier não tenha desenvolvido uma teoria atômica completa, suas contribuições experimentais foram cruciais para o desenvolvimento dessa teoria.
- Além de suas contribuições científicas, exerceu influência na administração financeira do governo francês, especialmente na reforma tributária.
- Casou-se com Marie-Anne Pierrette Paulze (1758-1836) em 1771, filha de um colecionador de impostos, e, além de ser sua esposa, ela desempenhou um papel significativo no trabalho científico de Lavoisier.

- Durante a Revolução Francesa, suas conexões com o Antigo Regime e a Ferme Générale, uma empresa de impostos, levaram à sua prisão e execução.
- Seu trabalho estabeleceu os fundamentos para a Química moderna e influenciou gerações subsequentes de cientistas.
- Lavoisier é frequentemente chamado de “pai da Química moderna” devido à sua influência duradoura na disciplina.
Ante ao exposto, a execução de Lavoisier durante a Revolução Francesa é frequentemente lamentada como uma tragédia, pois ele foi privado de mais contribuições valiosas para a ciência e a sociedade. No entanto, sua obra continua a ser uma pedra angular na história da Química. Saiba mais detalhes sobre a vida de Antoine Lavoisier clicando aqui.
Exercícios resolvidos sobre a lei de Lavoisier
Questão 1
Em um experimento químico, um cientista observou a reação de combustão completa de uma amostra de propano (C3H8) na presença de oxigênio (O2).
C3H8 + 5O2 → 3CO2 + 4H2O
De acordo com a lei de Lavoisier, qual é a expectativa em relação à massa dos reagentes e dos produtos?
A) A massa dos produtos será menor que a massa dos reagentes.
B) A massa dos produtos será maior que a massa dos reagentes.
C) A massa dos produtos será igual à massa dos reagentes.
D) A massa dos produtos e dos reagentes não está relacionada.
E) A massa dos produtos depende da temperatura da reação.
Resolução:
Alternativa C
De acordo com a Lei de Lavoisier, a massa total dos reagentes em uma reação química é igual à massa total dos produtos formados. Portanto, espera-se que a massa dos produtos seja igual à massa dos reagentes na combustão completa do propano.
Questão 2
Durante a combustão do carbono (C) em um recipiente fechado, 12 g desse elemento reagem com o oxigênio (O2) presente no ar, formando 44,0 g de dióxido de carbono (CO2). Segundo a lei de Lavoisier, qual a massa de O2 que havia no recipiente?
C + O2 → CO2
A) 32 g
B) 36 g
C) 12 g
D) 48 g
E) 18 g
Resolução:
Alternativa A
Segundo a lei de Lavoisier, a massa total dos produtos é igual à soma das massas dos reagentes. Sendo assim, a massa de O2 que reagiu será a subtração da massa de C da massa de CO2: 44,0 – 12,0 = 32,0 g. Portanto, a massa de O2 que reagiu foi 32,0 g.
Créditos das imagens
[1]Wellcome Trust / Wikimedia Commons (reprodução)
[2]Wellcome Trust / Wikimedia Commons (reprodução)
Fontes
AMERICAN CHEMICAL SOCIETY. The Chemical Revolution of Antoine-Laurent Lavoisier. Académie des Sciences de l’Institut de France in Paris, France, p. 14, 2015.
BASCUÑÁN BLASET, A. Antoine Laurent Lavoisier. El revolucionario. Educación Química, v. 19, n. 3, p. 226, 2011.
BERETTA, M. Imaging the experiments on respiration and transpiration of Lavoisier and Séguin: Two unknown drawings by madame Lavoisier. Nuncius, v. 27, n. 1, p. 163–191, 2012.
CARVALHO, R. S. Lavoisier e a sistematização da nomenclatura química. Scientiae Studia, v. 10, n. 4, p. 759–771, 2012.
CENTENO, S. A. et al. Discovering the evolution of Jacques-Louis David’s portrait of Antoine-Laurent and Marie-Anne Pierrette Paulze Lavoisier. Heritage Science, v. 9, n. 1, 2021.
DONOVAN, A. Lavoisier and the Origins of Modern Chemistry. Osiris, v. 4, p. 214–231, 1988.
III, J. E. M.; DONOVAN, A. Antoine Lavoisier: Science, Administration, and Revolution. The American Historical Review, v. 100, n. 4, p. 1258, 1995.
KARAMANOU, M.; ANDROUTSOS, G. Antoine-Laurent de Lavoisier (1743-1794) and the birth of respiratory physiology. Thorax, 2013.
NAGENDRAPPA, G. Antoine-Laurent Lavoisier. Resonance, v. 17, n. 1, p. 11–22, 2012.
REDEFOR - REDE SÃO PAULO DE FORMAÇÃO DISCENTE. A Lei de Lavoisier. Universidade Estadual Paulista, p. 1–3, 1789.
UNDERWOOD, E. A. Lavoisier and the History of Respiration. Journal of the Royal Society of Medicine, v. 37, n. 6, p. 247–262, 1944.
VIDAL, P. H. O.; CHELONI, F. O.; PORTO, P. A. O Lavoisier que Não Está Presente nos Livros Didáticos. Química Nova na Escola, n. 26, p. 29–32, 2007.
WENTRUP, C. Origins of Organic Chemistry and Organic Synthesis. European Journal of Organic Chemistry, v. 2022, n. 25, 7 jul. 2022.