Raio atômico
O raio atômico é uma propriedade periódica e pode ser definido como a metade da distância entre os núcleos de dois átomos vizinhos de um mesmo elemento.
Por Jennifer Rocha Vargas Fogaça

PUBLICIDADE
Medir o tamanho de um átomo é algo muito difícil porque a sua eletrosfera (região onde os elétrons ficam girando ao redor do núcleo) não possui um limite específico. Por isso, a forma mais comum é por meio do raio atômico, em que se considera o átomo como se ele fosse uma esfera (modelo atômico de Dalton).
Lembre-se de que, na Matemática, ao estudar sobre esferas, você aprendeu o que era raio e diâmetro. O raio é a distância compreendida entre o centro e a extremidade da circunferência e é a metade do diâmetro da circunferência, como mostrado a seguir:
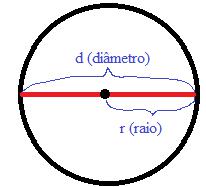
Diâmetro e raio de uma circunferência
Algo similar aplica-se ao conceito de raio atômico. Consideram-se dois átomos de um mesmo elemento químico como esferas que devem estar o mais próximo possível um do outro, sem estarem ligados quimicamente. O raio atômico (r) é a metade da distância (d) entre os dois núcleos desses átomos vizinhos.
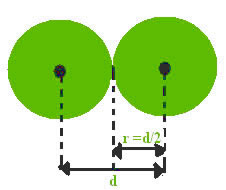
O raio atômico (r) é a metade da distância (d) entre dois núcleos de átomos vizinhos
Para conseguir essa medida, usa-se a técnica de difração por raios X. Nela, esses raios atravessam uma amostra de um material sólido de um único elemento químico (como um pedaço de ferro, pois ele é sólido e é formado somente por átomos de ferro), e os átomos ou íons que constituem esse material provocam um desvio na trajetória dos raios X. Depois os raios X incidem sobre uma chapa fotográfica e registram a posição dos núcleos dos átomos no material e a distância entre eles. Assim, basta dividir esse valor por dois para obter o raio atômico, que, em geral, é medido em nanômetros (1 nanômetro é igual à bilionésima parte de um metro (10-9 m)).
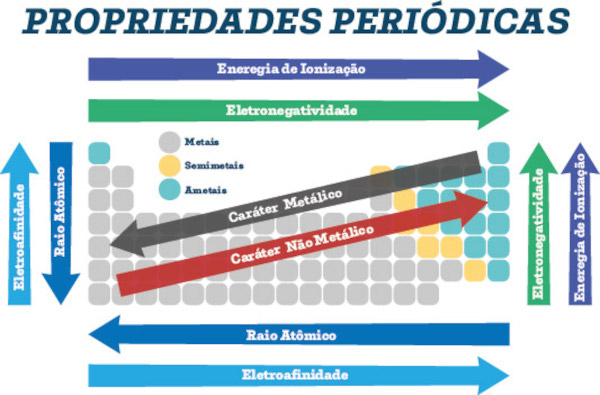
O raio atômico é uma propriedade periódica porque ele varia periodicamente em função dos números atômicos. Podemos dizer que, na tabela periódica, o raio atômico dos elementos cresce de cima para baixo e da direita para a esquerda:
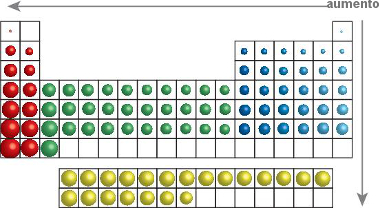
Sentido do crescimento do raio atômico na tabela periódica
Para entender porque o aumento do raio atômico segue essa ordem periódica, considere separadamente os elementos de uma mesma família e de um mesmo período:
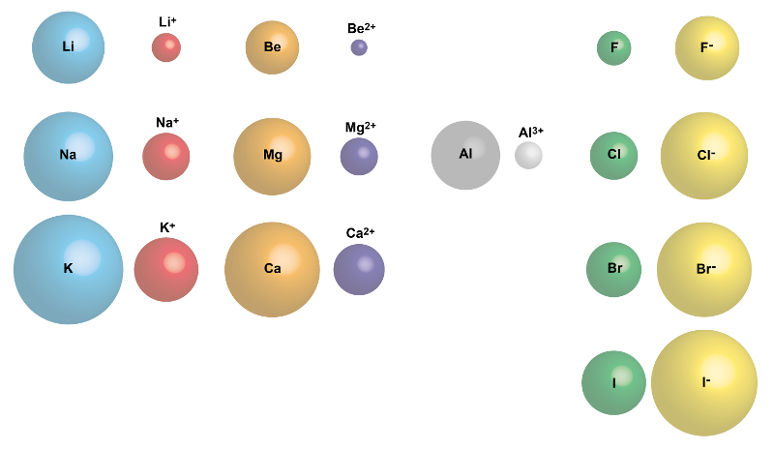
* Elementos de uma mesma família: De cima para baixo vai aumentando o número de camadas eletrônicas. Por exemplo, na família 1, o hidrogênio possui uma camada, o lítio possui duas camadas, o sódio possui três camadas e assim sucessivamente. Nesse sentido, aumenta também o número atômico e, por isso, o raio do átomo também aumenta.
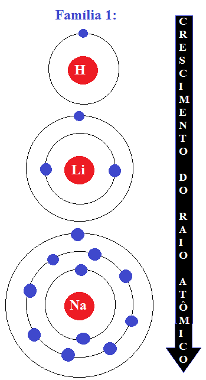
Crescimento do raio atômico em uma mesma família: de cima para baixo
* Elementos de um mesmo período: Da esquerda para a direita a quantidade de elétrons na camada de valência (camada mais externa ao núcleo) vai aumentando e todos possuem a mesma quantidade de camadas. Por exemplo, o potássio (K) possui quatro camadas eletrônicas e dezenove elétrons, o cálcio (Ca) possui também quatro camadas eletrônicas, mas apresenta vinte elétrons, o escândio (Sc) também possui quatro camadas eletrônicas, mas possui 21 elétrons, e assim por diante. Quando a quantidade de elétrons aumenta, a sua atração pelo núcleo, que é positivo, também aumenta. Assim, nesse sentido, em razão da atração entre o núcleo e a camada de valência, há uma contração do átomo, o que causa a diminuição do raio atômico. É por isso que o átomo cresce no sentido contrário: da direita para a esquerda.
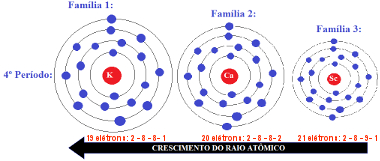
Crescimento do raio atômico em um mesmo período: da direita para a esquerda
Por Jennifer Fogaça
Graduada em Química