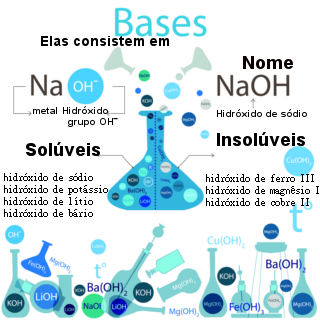
Solubilidade das bases
A solubilidade das bases está relacionada com a capacidade que essa substância apresenta de se dissolver muito, pouco ou quase nada em água.
Por Diogo Lopes Dias

PUBLICIDADE
Além da capacidade de dissociação (força das bases) e da quantidade de hidroxilas, as bases podem ainda ser classificadas de acordo com a solubilidade que elas apresentam em relação à água. Vale ressaltar que a solubilidade é a capacidade que um material possui de se dissolver em outro material.
Em relação à solubilidade, as bases podem ser classificadas em:
1) Base solúvel: é a base que apresenta uma ótima solubilidade em água.
Para determinar se uma base é solúvel, basta verificar se ela apresenta um cátion que pertence à família IA (metais alcalinos: Li, Na, K, Rb, Cs, Fr) ou se apresenta o cátion amônio (NH4+).
Exemplos:
-
Hidróxido de sódio (NaOH)
-
Hidróxido de potássio (KOH)
-
Hidróxido de lítio (LiOH)
-
Hidróxido de rubídio (RbOH)
-
Hidróxido de amônio (NH4OH)
2) Base pouco solúvel: é a base que apresenta uma baixa solubilidade em água. Quando adicionamos esse tipo de base em água, fica perceptível um material sólido que não se dissolveu no fundo do recipiente.
Para determinar se uma base é solúvel, basta verificar se ela apresenta um cátion que pertence à família IIA (metais alcalinoterrosos: Be, Mg, Ca, Sr, Ba, Ra).
Exemplos:
-
Hidróxido de magnésio [Mg(OH)2]
-
Hidróxido de cálcio [Ca(OH)2]
-
Hidróxido de estrôncio [Sr(OH)2]
-
Hidróxido de bário [Ba(OH)2]
3) Base praticamente insolúvel: é a base que apresenta uma baixíssima solubilidade em água. A quantidade de material sólido dissolvido é tão pequena que muitos autores chegam até a desconsiderar essa solubilidade. Quando adicionamos esse tipo de base em água, a impressão que temos é a de que não houve dissolução.
Para determinar se uma base é praticamente insolúvel, basta observar se o cátion presente na base não pertence às famílias IA, IIA ou se ele é o cátion amônio.
Exemplo 1: Hidróxido de prata (AgOH)
O cátion presente nessa base é a prata, um elemento químico que pertence à família IB. Logo, trata-se de uma base praticamente insolúvel.
Exemplo 2: Hidróxido de ouro III [Au(OH)3]
O cátion presente nessa base é o ouro, um elemento químico que pertence à família IB. Logo, trata-se de uma base praticamente insolúvel.
Exemplo 3: Hidróxido de ferro II [Fe(OH)2]
O cátion presente nessa base é o ferro, um elemento químico que pertence à família VIIIB. Logo, trata-se de uma base praticamente insolúvel.
Exemplo 4: Hidróxido de titânio IV [Ti(OH)4]
O cátion presente nessa base é o titânio, um elemento químico que pertence à família IVB. Logo, trata-se de uma base praticamente insolúvel.
Aproveite para conferir nossas videoaulas relacionadas ao assunto: