Saponificação
A saponificação é uma reação de hidrólise alcalina de ésteres de ácidos graxos por meio da qual ocorre a produção do sabão.
Por Stéfano Araújo Novais

PUBLICIDADE
A saponificação é uma reação de hidrólise de ésteres de ácidos graxos (como óleos e gorduras) em meio alcalino (básico), com a finalidade de produção de sabão (sais de ácidos graxos), tendo como subproduto o glicerol. Em geral, utiliza-se hidróxido de sódio ou hidróxido de potássio para essa reação, a qual necessita de um pequeno aquecimento para ocorrer.
A saponificação ocorre por um mecanismo de adição nucleofílica, seguida por eliminação no carbono acílico. Um parâmetro de qualidade importante para os sabões é o índice de saponificação, utilizado para mensurar quantos miligramas de base são usados para saponificar um miligrama de óleo ou gordura. A origem do processo de saponificação é incerta, porém é sabido que se iniciou pela mistura de cinzas vegetais com gordura animal.
Leia também: Qual é a composição química do sabão?
Resumo sobre saponificação
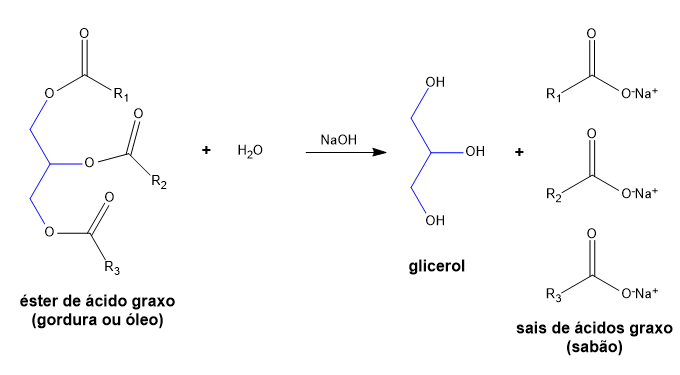
- A saponificação é uma reação de hidrólise alcalina de um éster de ácido graxo (gordura ou óleo), com a produção de sais de ácidos graxos (sabão) e glicerol.
- O sal de ácido graxo é um produto de caráter anfifílico, ou seja, tem caráteres polar e apolar bem desenvolvidos.
- Em geral, utiliza-se o hidróxido de sódio ou o hidróxido de potássio como substância alcalina na saponificação.
- A saponificação ocorre por meio de um mecanismo de adição eletrofílica, seguido por uma eliminação no carbono acílico (da carbonila).
- O índice de saponificação é a quantidade, em miligramas, de base necessária para se saponificar 1 miligrama de óleo ou gordura.
- A origem do processo de saponificação é incerta, porém sabe-se que se iniciou pela reação entre cinzas de plantas e gordura animal.
O que é saponificação?
A saponificação é um caso específico da reação de hidrólise sofrida por ésteres em meio básico (ou alcalino), em que o produto final é sal orgânico de caráter anfifílico (caráteres polar e apolar bem desenvolvidos), o qual pode ser usado como sabão. A palavra sapo vem do latim e significa “sabão”. Já o termo hidrólise faz referência à “quebra pela água”, já que o sufixo -lise vem do grego, lysis, e significa “quebra”.
Como e quando ocorre a saponificação?
A saponificação, para ocorrer, necessita de um éster de ácido graxo (triglicerídeo), ou seja, gordura ou óleo. Sendo o triglicerídeo um éster, é possível sofrer hidrólise. Esta, ocorrendo em meio básico (NaOH ou KOH como principais fontes alcalinas, embora outras possam ser possíveis, como carbonatos de sódio e potássio, amônia e bases orgânicas nitrogenadas), dá origem ao glicerol e a sais de ácidos graxos (sabão). Em geral, a reação ocorre em aquecimento moderado (na faixa dos 60 °C).
Os sais de ácidos graxos, solubilizados após a reação, podem ser precipitados via adição de cloreto de sódio (NaCl). Após isso, o sabão será secado e posto em moldes para sua comercialização.
Para fins comerciais, o sabão pode receber algumas mudanças, como a adição de perfume (para odor), areia (para ação mais abrasiva/esfoliante), corantes (para colorações diferentes) e bolhas de ar (para que possa flutuar na água).
Exemplos de moléculas comuns em sabões são o estearato de sódio, o oleato de sódio e o linoleato de sódio.
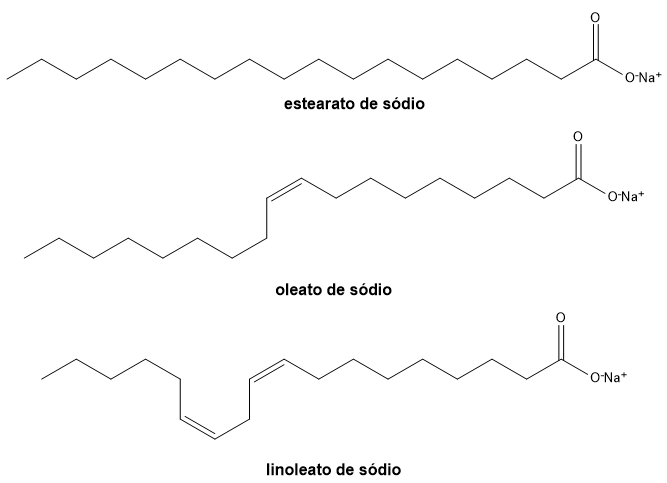
A carga negativa presente na carboxila (ânion carboxilato) faz com que a estrutura dos sais seja pouco reativa frente às reações de substituição nucleofílica. Assim sendo, é possível concluir que a reação de hidrólise alcalina é praticamente irreversível.
O mecanismo dessa reação envolve uma adição nucleofílica e uma eliminação no carbono acílico (o da carbonila).
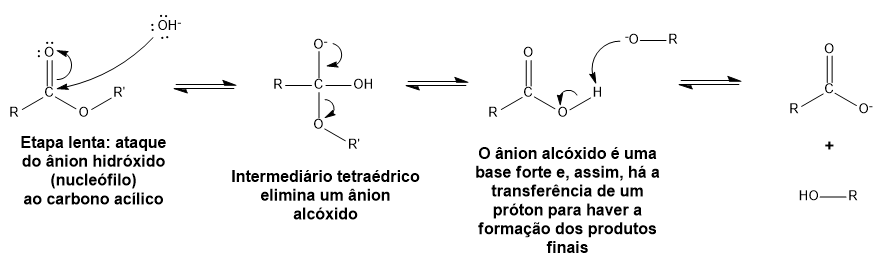
Tal mecanismo foi comprovado experimentalmente via marcação isotópica: nesse método, o oxigênio que atua como heteroátomo no éster é substituído pelo seu isótopo 18O. Ao fim do processo, percebeu-se que o isótopo estava ligado ao carbono acílico (da carbonila).
Veja também: Hidrólise de sais — processo de interação entre os íons do sal e da água
Índice de saponificação
Um parâmetro importante para o sabão produzido é o índice de saponificação. Esse índice se refere à quantidade, em miligramas, de base necessária para saponificar 1 grama de gordura ou óleo.
Esse índice acaba apresentando indicações acerca da composição do óleo (ou gordura) em termos de ésteres de ácidos graxos presentes. É sabido que ésteres de ácidos graxos de menor massa molecular requerem maiores quantidades de base para saponificação, e, portanto, conclui-se que o índice de saponificação é inversamente proporcional à massa molecular do triglicerídeo usado.
História da saponificação
A origem do processo de saponificação é incerta. Algumas fontes apontam para o ano de 2800 a.C., na Babilônia, outras, para o Egito, em 1500 a.C., e outras até mesmo para Fenícia, em 600 a.C. Contudo, é sabido que, desde os tempos antigos, o sabão surgiu da combinação de cinzas com gordura animal, uma mistura perfeitamente possível em abatedouros, sendo esse método reconhecido como o início da saponificação.
O sabão produzido foi inicialmente usado para lavagem de tecidos e roupas, e apenas posteriormente para higiene pessoal. O médico grego Galeano, que viveu entre 130 e 200 d.C., falava sobre a importância da utilização de sabão para a prevenção de doenças.
No século IX, o sabão deu um salto de qualidade, quando se adicionou azeite de oliva na sua manufatura. Sabe-se que o sabão dos tempos mais antigos não era esteticamente tão bonito, além de nem sempre apresentar bons odores. No século XVI, por exemplo, o sabão ainda era um artigo de luxo, apesar dos avanços nos processos de manufatura. A rainha Elizabeth I da Inglaterra, por exemplo, tomava um banho por mês apenas.
O sabão atingiu seu auge na segunda metade do século XIX e no começo do século XX, muito por conta de uma nova percepção acerca da higiene. Em 1847, o médico húngaro Ignaz Semmelweis percebeu que a lavagem de mãos por parte de profissionais que realizavam partos era uma forma eficaz de reduzir a taxa de mortalidade nas maternidades.
Por incrível que pareça, inicialmente, as ideias de Semmelweis foram desacreditadas por seus colegas médicos, até que Louis Pasteur apresentou suas descobertas e estudos acerca dos germes.

Foi nessa época também que a saponificação atingiu formas mais modernas de produção. Nicolas Leblanc criou um tipo de produção de soda (carbonato de sódio), o qual poderia ser obtido do sal (evitando assim o desmatamento). Esse método foi aprimorado por Ernest Solvay e permitiu a produção em larga escala de carbonato de sódio, usado como substância alcalina na produção de sabão. Com o tempo, o método de saponificação foi evoluindo, chegando-se à forma de produção atual.
Saiba mais: Qual a diferença entre detergente e sabão?
Exercícios resolvidos sobre saponificação
Questão 1. (Imepac/2019)
Antes do primeiro século d.C., os sabões, como conhecemos hoje, eram praticamente desconhecidos, e a fabricação deles quase não mudou em 2000 anos. As gorduras e óleos mais comuns na fabricação de sabões são toucinho e sebo, de fontes animais, e óleos de coco, palma ou oliva, de fontes vegetais.
Analise as afirmativas a seguir relativas à produção de sabões.
I. O processo de fabricação do sabão envolve a hidrólise ácida de uma gordura animal ou de um óleo vegetal.
II. As gorduras e os óleos são chamados triglicerídeos e o comprimento da cadeia carbônica está relacionado com as propriedades do sabão resultante.
III. Os produtos principais da fabricação do sabão são os sais de ácido carboxílico, que é o sabão, e o glicerol.
Estão corretas as afirmativas
(A) I e II, apenas.
( B) I e III, apenas.
(C) II e III, apenas.
(D) I, II e III.
Resposta: Letra C
O processo de fabricação do sabão envolve uma hidrólise básica (alcalina) e não ácida.
Questão 2. (Enem/2021)
A simples atitude de não jogar direto no lixo ou no ralo da pia o óleo de cozinha usado pode contribuir para a redução da poluição ambiental. Mas o que fazer com o óleo vegetal que não será mais usado? Não existe um modelo ideal de descarte, mas uma alternativa simples tem sido reaproveitá-lo para fazer sabão. Para isso, são necessários, além do próprio óleo, água e soda cáustica.
LOBO, I. Sabão feito com óleo de cozinha. Disponível em: http://pga.pgr.mpf.gov.br. Acesso em: 29 fev. 2012 (adaptado).
Com base no texto, a reação química que permite o reaproveitamento do óleo vegetal é denominada
(A) redução.
(B) epoxidação.
(C) substituição.
(D) esterificação.
(E) saponificação.
Resposta: Letra E
A reação orgânica descrita no texto, que produz sabão do óleo vegetal, com água e soda cáustica (NaOH), é conhecida como saponificação.
Fontes
BRUICE, P. Y. Organic Chemistry. 8. ed. Upper Saddle River, Nova Jersey: Pearson Education Inc., 2015.
DE CASTRO, H. F. Óleos e Gorduras. In: Processos Químicos Industriais II. Apostila 5. São Paulo: Universidade de São Paulo, Escola de Engenharia de Lorena, 2014.
JABONES BELTRÁN. History of Soap. Disponível em: https://www.jabonesbeltran.com/en/historia-del-jabon.html
SOLOMONS, T. W. G.; FRYHLE, C. B.; SNYDER, S. A. Química Orgânica: volumes 1 e 2. 12. ed. Rio de Janeiro: LTC, 2018.