Reações de hidratação em alcenos
As reações de hidratação em alcenos são fenômenos químicos de obtenção de álcoois a partir da adição de hidrônios e hidróxidos a um alceno.
Por Diogo Lopes Dias
PUBLICIDADE
As reações de hidratação em alcenos são, na verdade, uma modalidade de reações de adição. Assim sendo, para que elas aconteçam, é fundamental que a ligação pi existente entre os carbonos seja rompida.
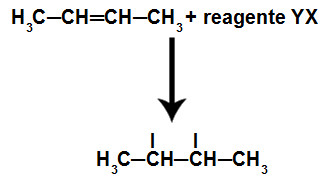
Representação do rompimento da ligação pi existente em um alceno
Nas reações de hidratação em alcenos, há a adição de dois componentes (Y e X) em cada uma das valências formadas após o rompimento da ligação pi.
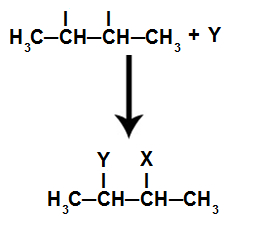
Como na reação de hidratação há moléculas de água, que sofrem o fenômeno da autoionização, formam-se os íons hidrônio (H+) e hidróxido (OH-).
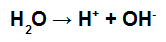
Equação que representa a autoionização da água
Assim, um dos carbonos que realizavam a ligação pi receberá o hidrônio (H+), e o outro carbono receberá o hidróxido (OH-)
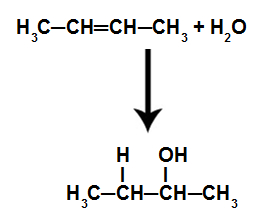
Para saber qual carbono receberá o hidrônio e qual receberá o hidróxido, basta utilizar a regra do cientista Markovnikov, que diz que:
-
O hidrônio (H+) deve ser adicionado ao carbono menos hidrogenados da dupla;
-
O hidróxido (OH-) deve ser adicionado ao carbono menos hidrogenados da dupla.
OBS.: Se o número de hidrogênios for o mesmo em ambos os carbonos da dupla, receberá a hidroxila o carbono terciário ou secundário.
Condições para a ocorrência das reações de hidratação em alcenos
-
Presença de um alceno como reagente;
-
Presença de água no meio;
-
Presença de ácido sulfúrico;
Não pare agora... Tem mais depois da publicidade ;) -
Aquecimento.
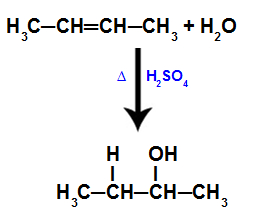
Equação geral de uma reação de hidratação em alcenos
Mecanismos de uma reação de hidratação em alcenos
-
1º mecanismo: autoionização da água, o que resulta na formação dos íons hidrônio e hidróxido;
-
2º mecanismo: quebra da ligação pi por meio do ataque realizado pelos íons provenientes da água e do aquecimento;
-
3º mecanismo: ligação do hidrônio (H3O+) a um carbono e a ligação do hidróxido (OH-) a outro carbono.
Exemplo de uma hidratação em alcenos
Para exemplificar as reações de hidratação em alcenos, vamos utilizar a hidratação do propeno (alceno com três átomos de carbono).
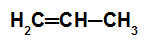
Fórmula estrutural do propeno
Quando o propeno é submetido a um meio com água, ácido sulfúrico e aquecimento, a ligação pi existente entre dois dos seus carbonos é rompida. O resultado disso é a formação de uma valência livre em cada um desses carbonos.
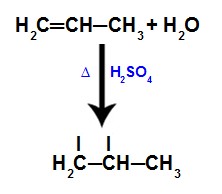
Representação do rompimento da ligação pi no propeno
Após a quebra da ligação pi, o hidrônio (H+) proveniente da autoionização da água liga-se ao carbono (carbono 1) menos hidrogenado que realizava a ligação pi, e o íon hidróxido (OH-) liga-se ao carbono (número 2) mais hidrogenado que realizava a ligação pi.
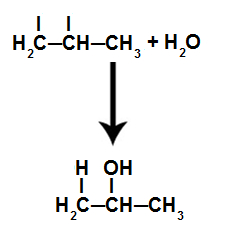
Equação que representa a formação do produto, que é um álcool
Por Me. Diogo Lopes Dias